Mark Bailey / Virus, Bacteriophage & Single “Virus” Genomics
ウイルス、バクテリオファージ、単一「ウイルス」ゲノミクス
マーク・J・ベイリー
2024/7/20
概念的なウイルスモデルは時代と共に変化してきたが、伝染病を引き起こす存在という根本的前提が確立されたことはない。にもかかわらず、ウイルスの支持者たちは、「バクテリオファージ」のような自然界に存在する粒子を、ウイルスと断定することなくウイルス学的領域に組み込もうと試みてきた。その一方で、技術の進歩が発見された理由であるかのように装っている。単一「ウイルス」ゲノミクスは、テクノロジー主導のウイルス学の世界において、法則化されたモデルの中に組み込まれたままである。
ウイルス
「ウイルス」の概念と意味は、数百年にわたり変遷してきた。ウイルスという言葉が英語に登場したのは14世紀のことであり、ラテン語で「毒、植物の樹液、ぬるぬるした液体、強力なジュース」を意味する「virus」に由来する[1]。1790年代には「感染症を引き起こす病原体」を指すようになり、近代的な科学的使用は1880年代に始まったと言われる[2]。ウイルスの最初の発見とされるものから、ウイルスとは何かについての一貫した定義はなかった。なぜなら、他の経験的な生物科学とは異なり、自然に観察され、記述され、単離され、病原性が検査できるような具体的なウイルス粒子は存在しなかったからだ。それゆえ、ウイルス学者が取り組むべき有形の財産が存在せず、ウイルスという用語は変幻自在の性質を帯び、最新のウイルス理論に追いつくために、あるプレタポルテ的(訳注:既製服的)な定義から次の定義へと移り変わることになった[3]。
ウイルス学の発展において広く見られるテーマとしては、目に見えない伝染性の実体が想像され、その後、間接的な観察によりその仮説が裏付けられたというものである。このタイムラインにおいては、タバコモザイクウイルスが1890年代に発見された最初のウイルスとされる。しかし、その最初の発見も、それ以降の発見も、現代の定義に合致するような「ウイルス」は示されていない。つまり、病気を引き起こし、複製能力を持ち、自然な曝露経路を通じて伝染する粒子である[4, 5](想像上の伝染性粒子自体は「ビリオン」として知られている[6])。
オランダの微生物学者マルティヌス・ベイエリンクは、タバコ・モザイク病の原因に関する1898年の論文のタイトルに、「contagium vivum fluidum(伝染性の生きた液体)」という言葉を使った[7]。彼はこの言葉を、可溶性だが当時の技術では可視化できない、微視的な感染因子の一種に関連するものと提唱した。1898年の論文の本文中では、ベイエリンクは「contagium」という用語を「ウイルス」と同じ意味で使っている。『Archives of Virology』では、新たな種類の病原体を意味するウイルスという言葉を初めて使ったのは彼の功績としているが、ベイエリンクと彼の同時代の人々は、今日知られているようなウイルスモデルを想定していなかったであろうことも認められている。
ベイエリンクの主張する伝染病の「流動性」は、彼がすでに「溶解性」と同じ意味で使っていたため、意味論上の問題である。彼が新たな種類の病原体に対して「ウイルス」という用語を作ったことは、生物学における新しい時代の幕開けを示すものだ。したがって、誰が最初にウイルスを発見したかを議論することはあまり有益ではない。どの先駆者も、自分が何を言っているのかわからなかったのだから[8]。
この謎めいた話題が、ウイルス学のパイオニアと呼ばれた人々の域をはるかに超え、現在に至るまで続いていることは明らかだ。ウイルス学は生物学の中でも特異な「科学」だが、それはウイルス学者が、自分たちが研究していると主張する実体の物質的性質を再定義する傾向があるからである。定義が変わったり、言語学的策略が用いられたりすることで、ウイルス学者自身はともかく、一般の人々にとっては、次の例が示すように、何を言っているのかわからなくなることがある。
「私の野望は、ウイルスという言葉が意味を持つと示すことであり、ウイルスはウイルスであるという逆説的な視点を守ることである」〜アンドレ・ルヴォフ、1957[9]
「…ウイルスとは、ウイルス学者が言うところのものである…ウイルス学者は、その科学の通常の進歩の一部として、ウイルスの概念を発明する(そして絶えず再発明する)と言える」〜ウィリアム・サマーズ、2014[10]
「人体やその粘膜の多くの宿主地区には、病気とは無縁のウイルスが多量に『コロニー化』している」〜論説、臨床微生物学と感染、2019[11]
「…コロナ・ウイルスはRNA分子の断片に過ぎない」〜ウィリアム・ローリンソン、2020[12]
ウイルス学者が何を言おうが、何を「正常な進歩」と考えようが、彼らが自然界でウイルスを発見し、その研究に着手したのではないことは明らかだ。作られたパラダイムは、その典型的な反証不可能な性質によって、反科学的な慣習に染まっている。なぜなら、ウイルスの物質的存在が常に事前に想定されているからである。どうやら、あとは細部を埋めるだけであるようだ。
「19世紀の微生物学者にとって、『ウイルス』は便利だが不正確な概念であった。ウイルスは、何であるかとの観点でなく、何をするか(病気を引き起こす、タバコの葉に病変を生じさせる、など)という観点で考えられていた」〜ウイリアム・サマーズ、2013[13]
ウイルスが「活動」するには、まず存在せねばならない。存在するなら、特定の生化学的組成と機能を持たねばならない。1800年代以降、ウイルスは前述の「流体伝染体」、化学物質、感染性タンパク質、亜細胞体などの性質を持つと仮定されてきた。ウイルス学者が現代的なウイルスの定義に落ち着き始めたのは1950年代になってからで、ゲノム(RNAまたはDNA)をコード化されたタンパク質の被膜が取り囲んだ伝染性の粒子という意味にである。
サルバドール・ルリアは、1953年に画期的な『一般ウイルス学』を出版したが、1957年に改訂した。確かにぎこちないウイルスの構造を(アンドレ)ルヴォフに書き送っている。「私は今日、ウイルスを『ウイルス自身の制御下で合成された伝達装置に組み込むことによって、伝達可能な形態をとることができる遺伝物質の要素』と定義したい」[14]。
物理的実体としてのウィルスの存在がいつ示されたのかとの疑問が残る。グッドパスチャー(Goodpasture)らは、1931年に「ニワトリ胚の絨毛-アラント膜における…ウイルスの培養」との画期的とされる発見を報告した[15]。しかし、培養された微生物の証拠はなく、彼らの主張は「膜上に発生し広がるワクチン性病変(vaccinal lesion)」の出現に依拠していた(強調は著者)。ここで、彼らは単に、病変の出現、すなわち損傷した膜組織は、導入したサンプルに存在するウイルスが起こしたに違いないと仮定した。論文の脚注によれば、彼らのサンプルは 「T.M.リバーズ博士の好意で提供されたレバディティ・ニューロワクチン(ウイルス)の一株」であった。
トーマス・リバーズ博士も同様に、提供したサンプルがこの「ウイルス」を含むと事前に主張し、1930年の公開物では、「ウサギの睾丸で6ヶ月間増殖させたレバディティ神経ワクチンウイルス」だと宣言した[16]。これらの実験のすべてにおいて、サンプルは混合生物学的標本であり、具体的な独立変数が特定されていなかったことは明らかだ(訳注:ウイルスそのものが特定はされていないとの意味)。グッドパスチャーもリバーズも、いわゆる「レバディティ株」の組成を知ることはできなかった(訳注:混合物の中に何があるのかわからなかった)。問題の組織は明らかに病気であり、そのウイルスが他の露出した組織に病気の徴候を示すのであれば、「ウイルス」の性質は「毒」という本来の意味以上のものであるとは言えなかった[17]。
これは初期のウイルス学者たちに対する不当な非難とされるかもしれない。彼らの実験は、1930年代後半に電子顕微鏡が利用可能になる以前から行われていたのだから。しかし、元ウイルス学者のステファン・ランカ博士が説明するように、新たなナノスケールのイメージング技術は彼らの問題を助けるものではなかったのだ。
ウイルスとは何か、という1951年以前の理論は、ウイルスに感染していると思われる人々や動物に、電子顕微鏡を使って、健康な被験者で発見できたり写真を撮れたりするものとは違うものを発見・撮影できなかった事実により反証された。これは今日でも同様である[18,19]。
1940年代から1950年代にかけて、ウイルス学者たちは間接的細胞培養法を好むようになった。この手法では、病気に罹患した生物の検体を、実験室で典型的な異常細胞株に加える。顕微鏡下で細胞が破壊されれば、ウイルスが原因と断定された。しかし、検体を加えなくても細胞が破壊されることを示すこともできる。つまり、その手順自体が同じ効果を引き起こす可能性があるのだ[20]。さらに、著者が『ウイルス学のイベントホライズン』(Virology’s Event Horizon)で論じたように、細胞培養法には論理的な欠陥がある。
(a) 「ウイルス性」と宣言された粒子は、CPE観測(訳注:検体を加えた細胞培養が破壊されること)の一部として初めて見られる。つまり、これらは従属変数である。同じ実験において、それらが独立変数でもあると主張するのは馬鹿げている。
(訳注:独立変数であるはずのウイルスは、実験開始時には全く検出されておらず、実験結果によってのみ「存在する」と主張される。したがって、この「科学実験」において、ウイルスは独立変数とはなりえない。つまり、「原因と結果」の原因は特定されていない)
(b) in vitro(実験室)での観察では、in vivo(生体内)のプロセスの再現はできない。
(c)電子顕微鏡に関わる技術は、対照化できないさらなる変数をもたらす。これが、技術的なアーチファクト(人工物)や、生体組織ではなく樹脂に埋め込まれた静的な構造物であるというさらなる制限に加えてである[21]。
ウイルス学におけるそれまでの実験方法論と同様、細胞培養技術はウイルスの存在を示すものではなかった。具体化の誤謬(reification fallacy、訳注:抽象的概念を具体的現実と混同して結論を導く)を永続させるだけであったのだ。つまり、想像上の概念が、確認された物理的存在であると不適切に宣言されたのである[22]。必要な証拠がないにもかかわらず、それ以前の時代の「ウイルス」という無形の原型が、これ以降、寄生能力を持つ個別の粒子であると宣言された。
電子顕微鏡画像は、そこから生きた細胞生物学について情報を得られるのかという点で、それなりの限界がある。たとえそうであっても、この限界の中では、この技術はウイルスモデルにとってもう一つの行き詰まりをもたらしたはずである。ウイルス性疾患に罹患していると言われる人々の直接検体(喀痰や血液など)において、期待された決定的な証拠を提示できなかった(再度[19]参照)。ウイルスを描写したと称する生物学の教科書に掲載される画像の増殖を可能にしたのは、細胞培養技術だけだった。しかし、その性質上、方法論を独立変数で制御することはできず、細胞破壊の外観に基づいて事後的に発明することは許されない。したがって、撮影された小胞構造のどれもが、外因性の病原性・伝染性の実体であるという証拠はない。
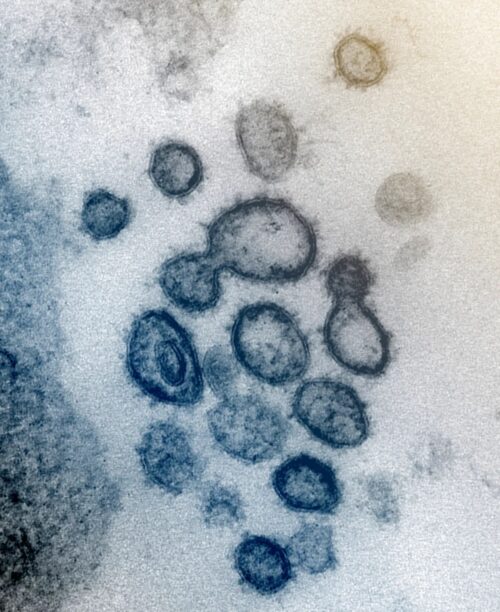
図1. 米国国立衛生研究所が2020年2月に公開した電子顕微鏡画像。SARS-CoV-2」のビリオンを示すとされる。これらの小胞の生物学的性質や組成をどのように決定したのかの根拠は示されていない。出典:https://www.chicagotribune.com/2020/04/04/know-that-coronavirus-image-with-red-spikes-heres-how-the-artists-atthe-cdc-created-it/
ウイルス学者たちは、図1に示した例のような電子顕微鏡画像において、「ポイント・アンド・デクレア」技術を採用している(訳注:単に矢印で指し示して、「これが✗✗ウイルスです」と宣言するだけ)。これらの粒子はSARS-CoV-2ビリオンと主張されているが、感染性や疾病の原因であるという確証はない。仮想のゲノムが構築されているが、画像化された粒子は精製されていないため、遺伝子配列の出所は不明のままである。混合物中の他の成分に由来する可能性もある(訳注:「ウイルスのゲノム」とされるものは、雑多な混合物中のすべてのゲノムを切り刻んで組み立て直したものに過ぎず、その出所は一切不明)。しかし、たとえ精製され、生化学的要素が決定されたとしても、自動的にウイルスとして認定されるわけではない。分離された粒子は、対照化された実験において、独立変数として要求される特性を示す必要があるのだ[23]。ゲノミクスがウイルスの存在を証明するという主張は、ウイルスの存在があらかじめ分かっているとの主張と同じ論理的誤謬に陥る。ウイルス学においては、これは細胞培養とメタゲノム(例えば、臨床サンプルの塩基配列決定)の両方に当てはまる。ウイルスが最初に存在することが示されない限り、「ウイルス」配列は存在し得ない。
ウイルスモデルの中心的な信条は循環論法の誤謬に陥っており、その支持者はそれに対処する気がないように見える。2014年、『Annual Review of Virology』誌には次のように書かれている。
ウイルスが疾病伝播の物質的基盤であるという基本的な考え方は、過去150年間ほとんど変わっていない。変わったのは、ウイルスの本質的な性質と生物学的能力についての理解である。ウイルスの概念は、特に科学的理解よりもむしろ技術の進歩によって決定されてきた[24](強調著者)。
しかし、この「基本的な考え方」が確立されたことはなく、科学的な方法に従えば、「ウイルス」という概念は1800年代のままである。つまり、なぜ生物が病気になるのかを説明しようとする精神的な概念である。目に見える独立変数がなければ、他の間接的な観察や技術開発をしても、このモデルをこの致命的な証拠の欠落から救うことはできない。
バクテリオファージ
バクテリオファージとは、文字通りバクテリアを食い荒らす、あるいは食べるという意味である[25]。この言葉は、1917年にフェリックス・デレルが「志賀菌(赤痢菌)に対する拮抗作用を持つ目に見えない微生物を単離した』と宣言したときに作られた[26]。 物理的な分離を証明したわけではなかったので、逆説的とまではいかないまでも、ナンセンスな発言であった。「目に見えない微生物」はまたもや具体化の誤謬を引き起こしているが、彼は言語的な手品によって精神的構成を実体化しようとしたのである。にもかかわらず、この話はウイルス学の権威に受け入れられ、2010年版の『Desk Encyclopedia of General Virology』には、「デレルは自分がウイルスの新たなカテゴリーを発見したことをすぐに理解した」と書かれている[27]。
デレルの「抗志賀菌」は、培地に糞便を4、5滴加え、37℃で18時間培養した後、チャンバーランド・キャンドルフィルター(バクテリア細胞を除去する)を通して作られた[28]。この無細胞濾液を赤痢菌の培養液に加えると、赤痢菌の増殖が阻害され、溶菌することが観察された。他のウイルス学者と同様、彼はバクテリア培養での観察結果の原因説明のため、バクテリオファージという架空の存在を作り出しただけだった。寄生性の「目に見えない微生物」があるとの推測に疑問を持つことなく、彼はその後のすべての観察を、未確立の自分の前提に合うようにし続けたのである。
拮抗微生物は赤痢菌のいない培地では決して培養できない。加熱死させた赤痢菌を攻撃することはないが、生理的食塩水中の洗浄細胞の懸濁液では完全に培養される[29]。
現代の(論文)著者たちは、デレルの主張を疑う余地のない科学的事実であるかのように宣伝し続けている。その中には、想像上のバクテリア「ウイルス」に目的論的な性質を与えてまで、この話に独自の付加を加えた者もいる。
(ディレルは)すぐに、バクテリオファージはバクテリアが繁殖する場所であればどこにでも存在することを知った。下水道、パイプから流出する廃棄物を受け止める河川、そして回復期の患者の便の中である。他の捕食者と同じように、バクテリオファージは餌の近くにいるときに最もよく生き残り、増殖することができる。そこでバクテリアを抑制するという進化の役割を果たすのである[30]。
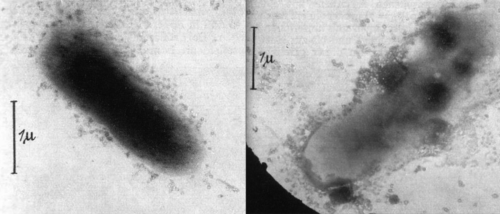
図2. 大腸菌の表面を攻撃していると想像される「コリファージ」の1940年に発表された最初の電子顕微鏡写真の一部。出典:https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3626388/figure/F1/
バクテリオファージとされるものを示す最初の電子顕微鏡写真は、1940年にドイツの2つの論文で発表された。Bacteriophage誌によれば「バクテリオファージの粒子性を証明した」という[31]。ある論文では、「大腸菌のブロス培養液に溶菌液を加えた」混合物の画像化について述べている[32]。図2にその論文からの2つの画像を示す。細胞の周囲にある小胞状の粒子は、おそらく事前にウイルス性であることが決定されていたと思われる。この粒子がもともと内因性のもので、細胞が破壊された結果生じたものであるという可能性は、著者たちは結論において考慮しなかったようである。
1940年のもう1つの論文は、「大腸菌のブロス培養液を濾過したバクテリアを含まないファージ溶解液」の電子顕微鏡画像について報告している[33]。この画像では、直径60ナノメートル前後の均質な粒子を示すいくつかの証拠が得られた。しかし、最初の論文と同様、これがウイルス性であることを示す証拠はない。
細胞膜溶解の沈殿物質には多くのものが知られている。加圧、加熱、浸透圧ショック、アルカリ暴露、洗剤、酵素のほか、音波、光学的、電気的刺激などだ[34]。図3は、18アミノ酸長の破壊ペプチドであるpVECに暴露された大腸菌細胞の破壊を示している。細胞を取り囲む粒子は、この例では「バクテリオファージ」とは呼ばれていない。
2015年、ステファン・ランカ博士は、なぜウイルス学者が捕食性のバクテリア「ウイルス」についての先入観から、画像を解釈する際に誤った結論を導き出したのかについて概説した。
発見当時はまだ目に見えなかったこれらの構造体がバクテリアを殺すという信念から、ファージ/バクテリオファージ、すなわち「バクテリアを食べるもの」と呼ばれた。しかし後になって、高度に近親交配された、つまりほとんど生存不可能なバクテリアがファージに変わること、あるいは芽胞を形成する時間がないほど急速に破壊されるバクテリアがファージに変わることが判明した[35]。
バクテリオファージは、自然界で発見され、単離され、特性決定される限りにおいて存在する。バクテリオファージは、バクテリアが存在するあらゆる場所で見つけることができるし、これからも見つかるだろう。海では、108個/mlものバクテリオファージが確認され、ファージデータベースには何千ものバクテリオファージが登録されている[36]。ファージは「バクテリアを食べる」粒子ではなく、微生物学的システムにおける環境変化に対する反応の一部である内因性要素であるとしか言いようがない。
ウイルス学者たちは病原性ウイルスの存在を示せず、まずバクテリオファージがウイルス性であると主張し、次にヒトのような大きな生物を攻撃する同等のウイルス粒子が存在するとほのめかすことで、その誤りをさらに深めている[37]。
単一「ウイルス」ゲノミクス
フローサイトメトリーとは、流体試料を細いシースに通すことで、単一の生体細胞を分析する技術である。レーザー光線がシースに照射され、検出器が光信号とインピーダンス信号を受信する。これが細胞に関する情報を提供する[38]。フローサイトメトリー装置の中には、特定の種類の細胞を物理的に分離するために使えるものもある。フローサイトメトリーは、医療診断や科学研究において数十年にわたり使われてきたツールである。
1980年代までに、フローサイトメトリーは、天然水サンプル中の微細な植物プランクトンの定量化に使われるようになった[39]。1990年代には、「フローサイトメトリー(FCM)を用いて海水中のウイルスを定量化することに成功した」とされた[40]。しかし、測定された「ウイルス」は、植物プランクトンに関連する「ビリオプランクトン」またはバクテリオファージであるフェオシスチスクラスであった。ウイルス学者たちは、またもや実質的な証拠なしに、バクテリオファージは微生物のライフサイクルというよりもむしろ「感染」サイクルの一部であるとして、ウイルス性であると宣言した。2000年に発表された論文のような総説は、微生物が活動しているところならどこでも、バクテリオファージも活動していると指摘し続けている。
水生ウイルスについては、これまで調査されたほぼすべてのケースで、その個体数はバクテリアプランクトンの濃度と最も強い相関関係があった。さらに、バクテリアの生産性が高い条件下では、より多くのウイルスプランクトン集団が見られるようである。多くの著者は、バクテリオファージがビリオプランクトン個体群の大部分を占めていると推測している。したがって、水生ウイルスの個体数が、バクテリオプランクトンの個体数および活性と密接な相関関係があることは驚くべきことではない[41]。
ステファン・ランカ博士が説明しているように、自然界に存在する明確な物理的粒子としてのバクテリオファージと巨大ウイルスの存在は疑問視されていない。しかし、これら2つの関連する存在の名称は誤用であり、その生物学的役割が寄生であるとは示されていない。
…いわゆる巨大ウイルス、すなわち、海中や基本的な生物であればどこにでも存在する、核酸を包んだものである。他のバクテリオファージと同様、無害であるばかりでなく、有益な機能を有している。ファージは密度勾配遠心分離法によって単離することができ、その存在が証明されている[42]。
このように、生物学的パラダイムが無視される中、フローサイトメトリーのさらなる発展により、2011年の『Public Library of Science』誌で「シングルウイルスゲノミクス」(SVG)が発表された[43]。「SVGの利点は広範囲に及び、様々な臨床や環境における新規ウイルスの発見を可能にする…」と主張された[44]。この技術により、アガロース液滴中に単一粒子が分離され、共焦点レーザー走査型顕微鏡で確認された。単離された粒子はゲノム増幅によってDNA配列が決定された。信じられないような技術の勝利かもしれないが、この論文は実際にこれらの粒子がウイルスであることを証明したわけではない。試験された 「ウイルス 」懸濁液は、大腸菌T4とλバクテリオファージであった。その性質については、本稿ですでに述べたとおりである。
病理学的な微生物としてのウイルスが存在することが示されない限り、SVGは「ウイルス発見」を可能にはできない。「ウイルスとはウイルス学者が言うものである」という同語反復的な宣言は、科学的に破綻したパラダイムを物語っている。人類は、ウイルス学者が伝染性で病気を引き起こす微生物を研究していると信じ込まされてきた。ゲノミクス、プロテオミクス、電子顕微鏡写真、疑惑の診断テスト、疫学データに関する情報が氾濫している。ウイルス学者たちは、このようなデータが19世紀に最初に考え出されたモデルに合致し続けると信じているかもしれないが、このような想像は生物学的現実とは何の関係もない。
(リファレンスは原著を参照のこと)


コメント
NHKや民放が放送した特番でみる陰謀
ウイルスと同じ大きさのエクソソームは撮影できる
コロナウイルスとエクソソームは見分けがつかない
エクソソームとは何ですか?
アンドリュー・カフマン博士も言っていたエクソソーム
生命維持の要 エクソソーム (NHK サイエンスZERO)
癌エクソソームの注射はどうですか?
スターゲートが気になる
秘密裏に人を殺したいなら良い方法かも
すかさずロスチャイルドの代理人ジャック・アタリの提言、世界政府をすり込むNHK
世界政府を提言するジャック・アタリ (NHK マネー・ワールド 資本主義の未来)
苔らの泉 odysee.com
COVID 19 – 世界的な詐欺の証拠
世界政府を提言するジャック・アタリ (NHK マネー・ワールド 資本主義の未来)
精神改造 恐怖の洗脳計画 MKウルトラ (NHK フランケンシュタインの誘惑)
ドルの時代の黄昏 〜アメリカ金融危機と基軸通貨の終焉~ (NHK BS世界のドキュメンタリー)
ゲノム編集食品その実態と安全性は?狙われる日本の農産物「種子法」(BS11)
NHKが報道してきたのは、我々の注意を集中させたい公式の言説だけだ。そのいわゆる専門家が、国家やNHKが私たちに信頼させたい意見に、奴隷のようにオウム返しにしたり、適合させたりするため、NHKは専門家と見なしている。反対意見の「専門家」分析は、NHKによって無視されるか、中傷されるかのどちらかです
国民の敵NHKはすべて分っていて実行しました。検閲産業複合体です。 司令塔のWEF年次総会ダボス会議にも大金を払って参加しています。
Mark Carney 現カナダ首相を調べる
史上最大の詐欺を見る
「グローバル金融ガバナンス」の新しいシステムを構築する。そして、同盟加盟国の利益にとって「友好的」と見なされるビジネス環境の確立を開発途上国に強制することにより、開発途上国の国家主権を侵食します。言い換えれば、このグループを構成する強力な銀行関係者は、持続可能性の促進を装って、自分たちの利益のために世界の金融システム全体を再構築しようと推進しているのです。
1京5000兆円規模の世界金融同盟を発表 (テレ東BIZ)
テレ東BIZ 記事の解説 ↓
COP26を隠れ蓑に、世界で最も強力な民間金融利害関係者は、世界銀行などの機関と融合し、それらを利用して発展途上国の国家主権をさらに侵食することで、世界の金融システムを変革する計画を策定しました。
それは確かに国連に対する一般的な一般の認識ですが、この組織は何十年もの間、民間部門と億万長者の「慈善家」を中央政府よりも特権を与える「利害関係者資本家」モデルに従っており、後者は単に前者によって作成された、そして前者の利益のために作成された政策のための「可能な環境」を作り出す任務を負っています。
1998年の世界経済フォーラムで講演したコフィ・アナン事務総長は、この変化を明確にした。
「国連は、ここダボス会議で最後に会合して以来、変化しました。組織は、私が「静かな革命」と表現した完全な見直しを受けました。根本的な変化が起こりました。国連はかつて政府とのみ取引していました。平和と繁栄は、政府、国際機関、ビジネス界、市民社会が関与するパートナーシップなしには達成できないことを私たちは知っています。国連の事業は世界の事業に関係しています。」
国連が支援するバンカー・アライアンスが世界の金融システムを変革する「グリーン」計画を発表
最近カナダの新首相に選出されたマーク・カーニー氏は、自身もネット・ゼロ・バンカーマンだった。むかしむかし、彼はイングランド銀行の総裁であり、地球を救うことに情熱を注いでいたため、グラスゴー・ファイナンシャル・アライアンス・フォー・ネット・ゼロ(GFANZ)と呼ばれる銀行家のカルテルを設立しました。2021年以降、これは国のエネルギー政策を吸い込むブラックホールでした。ある時点で、GFANZのすべての銀行家は累積で130兆ドル相当の資産を管理していました(これはTで1兆ドルに相当します)は、米国経済の5倍の規模であったことを意味します。それだけでは十分ではないかのように、彼らは国連と共謀し、本質的に準世界政府のように振る舞い、目標とルールを設定し、合法的な石油・ガス会社への融資をボイコットすることで民主主義国家を支配していた。GFANZは最終的に、米国の共和党19州によって去勢され、法的な独占禁止法と受託者義務の一斉射撃を仕掛けた。
もちろんジュネーブの(WHO)、ロンドンの国際気象機関事務所、ワシントンの国際通貨基金と世界銀行の事務所、オランダの国際刑事裁判所、ローマの他のいくつかの事務所など、国連機関の20の異なる世界事務所を示すスライドで彼の発言を説明し、国連機関がほとんどの人が認識しているよりも世界の風景に点在しているのと同じように、そのような遠く離れた国連管理拠点から多額の債務を抱え、国境を打破するための国連支援のさまざまな計画が生まれている点を強調しました。
タルサのレッドピルエキスポで強調された国連80歳およびその他の重要なトピック|UKコルム
大ヒット作:マーク・カーニー氏ネットゼロバンカー自身は、現在、石油、ガスを使用してカナダをエネルギー超大国にする« JoNova
マーク・カーニーとチャールズ国王の影響下で、イングランド銀行とロスチャイルド・シティ・オブ・ロンドンの金融網で最も汚い銀行のいくつかは、グリーンボンドが主導する「グリーン金融商品」を推進し、年金制度や投資信託を、正気の人なら誰も意図的に投資しないグリーンプロジェクトに向け直しました[強調を追加]。カーニーはまた、リン・フォレスター・ド・ロスチャイルド、チャールズ3世、教皇フランシスコと緊密に協力し、2020年12月にインクルーシブ・キャピタリズム評議会をバチカンと統合しました
カーニーの星がもっと高く上がれないかと思われたその時、カナダのテクノクラートは王立国際問題研究所(別名チャタム・ハウス)の所長に任命された。まだ知らない人のために説明すると、チャタム・ハウスは、ヒラリー・クリントンが2011年に「母船」と名付けた外交問題評議会の支配者である。この母船と世界的なシンクタンクは、ローズ・トラストによって創設され、大英帝国を一つの世界政府の王座として回復し、失われた米国の植民地を取り戻すという明確な目的を持って設立されたローズ・ミルナー円卓会議運動の機能を引き継いだ。
1877年の遺言で、セシル・ローズでさえ、「イエズス会憲法」を中心に大英帝国の新しい教会をモデルにするよう呼びかけ、ファビアン協会は、文化、好み、政治のあらゆる手段に影響を与えるために、この浸透理論の方法に直接その技術をモデルにしました。
モーリス・ストロングの幽霊は、マーク・カーニー・テクノクラシーでカナダに出没します |UKコルム
彼の履歴書のハイライトを見てみましょう。
• 1990-2003年:ゴールドマン・サックス(各種)
• 2003-2007年:カナダ財務省(上級副大臣)
• 2007-2013年:カナダ中央銀行(会長)
• 2010-2012年:国際決済銀行 国際金融システム委員会(委員長)
• 2013-2020: イングランド銀行 (総裁)
• 2020-2024年:ブルックフィールド・アセット・マネジメント(副会長)
• 2020-2025年:国連気候変動対策・資金特使
• 2025-????: カナダ首相
ああ、そのリストにはたくさんの銀行がありますよね?チャタム・ハウスや世界経済フォーラムでの特別任命や、ビルダーバーグでの定期的な出演は言うまでもない。しかし、鋭い目を持つ人は、以前に選出された公職がなかった ことに気付くかもしれません。
マーク・カーニーの紹介 – カナダの次期(選挙で選ばれていない)首相 – OffGuardian
COP26を隠れ蓑に、世界で最も強力な民間金融利害関係者は、世界銀行などの機関と融合し、それらを利用して発展途上国の国家主権をさらに侵食することで、世界の金融システムを変革する計画を策定しました。
国連が支援するバンカー・アライアンスが世界の金融システムを変革する「グリーン」計画を発表
現在入手可能な事実に基づくと、ブラックロックは州民の苦労して稼いだお金を使って、可能な限り最高の投資収益率と投票を回避しているようです。ブラックロックの過去の公約は、化石燃料の段階的廃止を強制し、エネルギー価格を上昇させ、インフレを促進し、米国の国家安全保障を弱体化させるパリ協定などの国際協定を遵守するよう企業に圧力をかけるために市民の資産を利用してきたことを示している。
これらの協定は、米国上院によって批准されたことはありません。この国の市民によって選出された上院議員は、ブラックロックではなく、どの国際協定が法の効力を持つかを決定します。司法長官としての管轄権限に該当する追加の懸念事項がいくつかあります
米国19州、民間政府として機能しようとするブラックロックの厚かましい取り組みにうんざり |UKコルム
今日の言葉で言えば、この「予測モデリング」の実践は、中央銀行の大祭司(および国連気候変動対策と金融に関する特使)のマーク・カーニー氏が、2050年までに脱炭素社会を促進するための新しい金融システムを求める呼びかけに反映されています。カーニー氏が公言した緊急性は、二酸化炭素排出量との推定関係に応じて、世界は1.5度温暖になるという「予測モデル」に基づいている。カーニー氏らによると、これは炭素を収益化し、人間の産業活動を停止することで利益を上げる場合にのみ修正できるという。
ローマクラブと「予測モデリング」マフィアの台頭。
マーク・カーニーを検索しました – テクノクラシーニュース
検索 |UKコルム
「 マーク・カーニー 」の検索結果 – OffGuardian
1.我々、各国の元首及び政府首脳、閣僚、上級代表は、ニュー・アーバン・アジェンダ の採択を目的とし、広域地方及び地方政府、国会議員、市民社会組織、先住民や地 域社会、民間企業、専門家や実務家、科学・学術コミュニティ及びその他の関連する 利害関係者とともに、2016年10月17日から20日にかけてキトで開催された国連住宅及び持続可能な都市開発会議(ハビタットⅢ)に参加した。
ホームタウン事業とはこれですか?「ニュー・アーバン・アジェンダ」 : メモ・独り言のblog
「持続可能な開発」の起源 1976
国連ハビタット Ⅰ会議 – 私有地所有は持続可能ではない!
1976年5月31日から6月11日まで、カナダのバンクーバーで、国連は最初の「ハビタット」[ハビタット I] 会議を開催し、「バンクーバー人間居住宣言」が署名された。国連は、「急速な都市化の規模と影響」を認識し始めた。 これは、迫り来る国連のアジェンダにおける「持続可能性」を定義した最初の会議の一つです。
国連ハビタット 会議 – 私有地所有は持続可能ではない! : メモ・独り言のblog